隨著貫徹落實國辦《關于全面深化藥品醫療器械監管改革促進醫藥產業高質量發展的意見》的深入���,我國醫療器械行業的快速發展及政策環境的持續優化����,越來越多的跨國企業選擇將進口醫療器械轉移至中國境內生產���。通過分析2025年上海市器審中心對進口轉國產的有源醫療器械開展注冊現場核查的情況,有源醫療器械進口轉國產注冊體系不符合項主要集中在設計開發�、采購�、生產管理與質量控制部分,合計占比96.41%���。
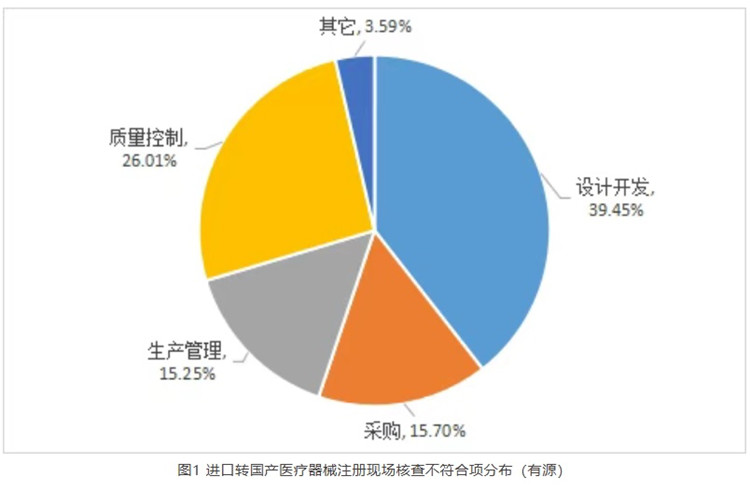
隨著貫徹落實國辦《關于全面深化藥品醫療器械監管改革促進醫藥產業高質量發展的意見》和《2025年穩外資行動方案》的深入,我國醫療器械行業的快速發展及政策環境的持續優化���,越來越多的跨國企業選擇將進口醫療器械轉移至中國境內生產��。通過分析2025年上海市器審中心對進口轉國產的有源醫療器械開展注冊現場核查的情況����,有源醫療器械進口轉國產注冊體系不符合項主要集中在設計開發、采購���、生產管理與質量控制部分�,合計占比96.41%���,如圖1所示����。
有源醫療器械進口轉國產醫療器械注冊體系常見問題設計開發
1、設計輸出:(1)部分技術圖紙缺失�,如產品總裝圖����、電氣連接圖、電路原理圖等;(2)設計輸出的物料清單與產品樣機的實際組成不一致;(3)產品設計輸出的技術參數與產品技術要求不一致;(4)產品說明書或軟件操作界面的相關內容未轉換為中文。
2、設計轉移:(1)產品由境外企業設計轉移而來��,但未與境外企業簽訂設計開發轉移協議����;(2)簽訂的轉移協議未明確轉移的技術文件清單和軟件版本信息、未明確軟件的變更與維護、配置管理等相關的要求和責任;(3)簽訂的轉移協議明確了轉移產品設計輸入和輸出資料,但現場未查見產品零部件圖紙、軟件安裝包等設計輸出文件。
3��、設計變更:(1)境外企業已對軟件進行了升級,但現場查見企業未對軟件版本升級的具體內容進行識別、評審和風險分析;(2)產品技術要求的軟件版本編碼規則與境外企業的規定不一致�,且未查見明確的編碼對應關系。
4��、設計驗證確認:(1)生物相容性評價����、產品有效期評價等直接使用境外企業的報告,并未從原材料/關鍵部件及生產工藝等同性等方面對上述報告的適用性進行評審�����;(2)設計驗證未考慮國內相關強制性標準���;(3)未對產品的全部工作模式進行測試。
如有有源醫療器械進口轉國產醫療器械注冊體系咨詢服務需求,歡迎您隨時方便與杭州證標客醫藥技術咨詢有限公司聯絡����,聯系人:呂工����,電話:18058734169,微信同����。